
骏马奔腾开胜景,春风浩荡展宏图
今天给大家介绍一种特别的“马”:它不在草原驰骋,而在我们的大脑里默默耕耘;它虽无奔腾之姿,却承载着记忆储存、认知调控的关键使命,是大脑中当之无愧的隐形功臣。它,就是海马体。
这匹“马”对我们大脑的正常运作具有重要意义。让我们看看,中国科学院脑科学与智能技术卓越创新中心(以下简称“脑智卓越中心”)的科学家们从它身上发现了什么吧。
海马体在哪里?
在我们大脑的深处,藏着一种小巧而弯曲的结构,它的形状与海洋中遨游的海马高度相似:弯曲的躯干、突出的头部与延伸的尾部相互衔接,整体呈C形蜷缩在大脑内侧颞叶,大脑的左右半球各有一枚(图1)。
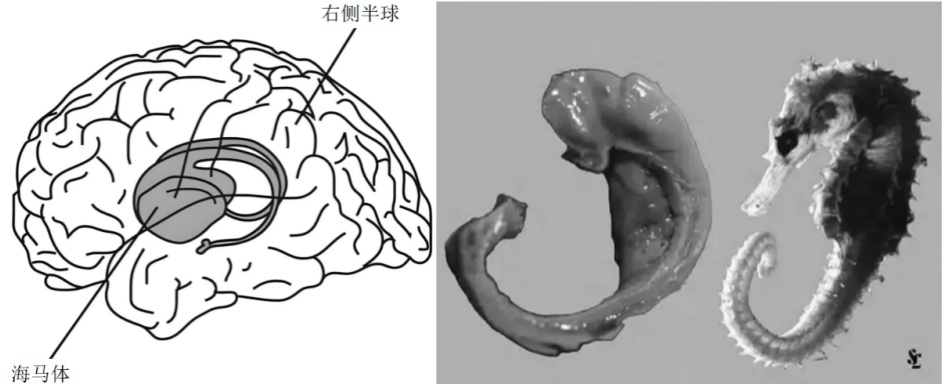
图1:大脑海马与动物海马对比图
(图片来源:《The Hippocampus Book》)
这一结构的命名可追溯至1587年,意大利解剖学家朱利奥·塞萨尔·阿兰齐首次将其称为“海马体”。功能探索则始于1953年,患者H.M.因癫痫手术切除双侧海马体后,丧失了形成新记忆的能力,这一病例首次证实海马体是记忆转化的关键中枢。在1971年,约翰·奥基夫在大鼠海马体发现位置细胞,证实其能构建空间认知地图;2005年,梅·布里特·莫泽与爱德华·莫泽夫妇在相邻的内嗅皮层发现网格细胞,补全了大脑定位系统的坐标机制。三人因揭示大脑 “内置“GPS”的细胞基础,共同荣获2014年诺贝尔生理学或医学奖,为人类理解空间导航与记忆机制奠定了里程碑[1]。
从结构上看,海马体从大脑背侧延伸到大脑腹侧(图2),由几个精密协作的区域组合而成,不同的区域有着不同的细胞类型、环路连接与对应的功能,海马体内部也充满了复杂的神经纤维网络[2]。
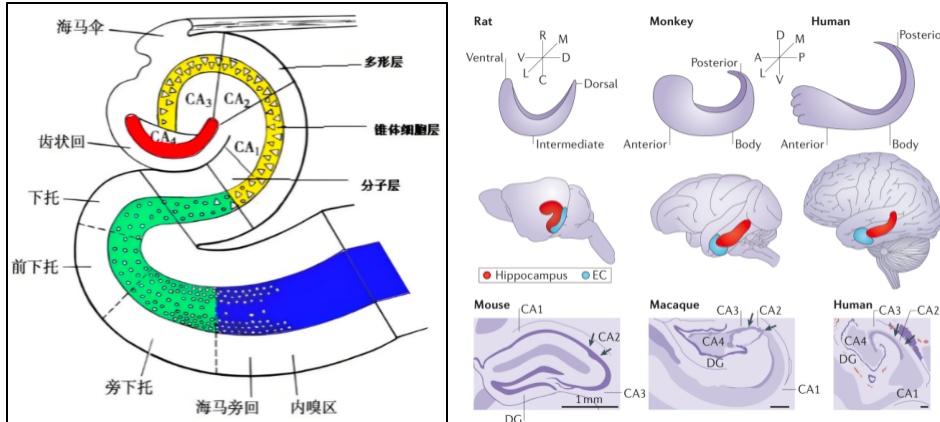
图2:海马体精细结构及背侧和腹侧海马
(图片来源:pixabay;[2])
是记忆宫殿,也是导航系统
提到海马体的主要功能,它就像我们个人记忆系统的核心枢纽,不仅帮助我们记住“是什么”,还能记住“在哪里”以及当时的情境,这对于我们在环境中导航定位也至关重要。
海马体最为人熟知的功能是其在记忆形成和巩固中的关键作用(图3)。海马体并不负责长期储存所有记忆,它是将新经历转化为持久记忆的核心转换站。
当你经历一件事,比如一次有趣的谈话、一次旅行的片段等,海马体会迅速收集来自感官的碎片信息,然后将这些元素精巧地编织成一个完整、连贯的“情景记忆”包,在记忆包贴上关键的“索引标签”,并将它发送到大脑皮层的不同区域进行长期储存。当你日后回忆时,海马体又根据一丝线索快速调取“索引标签”,帮你从大脑庞大的“记忆档案馆”里取出完整的场景。正是海马体日复一日地编辑与整理,将我们流动的体验固化成了可以回溯的人生故事。
而海马体受损的人,虽然能记得很久以前的事,却很难记住新的对话或刚刚发生的事情,因为他们的“当下”无法被有效编织和储存。
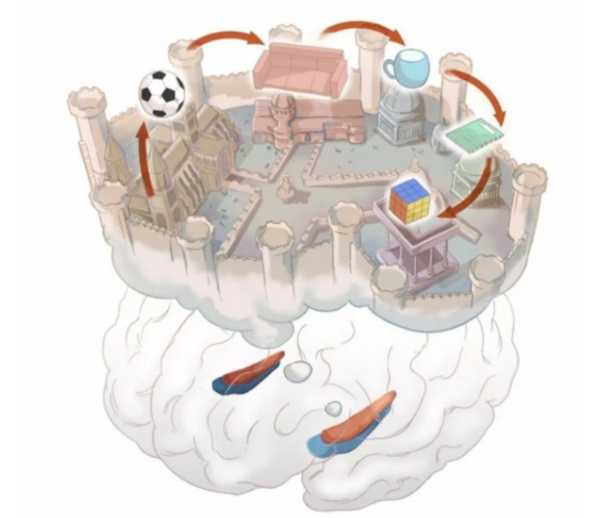
图3:海马体能够将新事物、新经历转化为记忆
(图片来源:北京师范大学认知神经科学与学习国家重点实验室官网)
同时,海马体还负责空间信息和导航处理,该能力依赖于其内部及周边神经网络中一系列高度特化的神经细胞协同运作,其核心是海马体中的“位置细胞”与内嗅皮层的“网格细胞”(图4)。
海马体就像大脑里一个神奇的“体感录像机”。当你来到一个新地方,一群位置细胞会标记和连接每一个地点,在脑内构建空间关系。更厉害的是,它与内嗅皮层的网格细胞联手,能够把位置、时间、事件和当时的感受编织在一起,形成一个完整的情景记忆。正是海马体无声无息地记录与珍藏,将你走过的山河编织成了可以回味的岁月篇章。
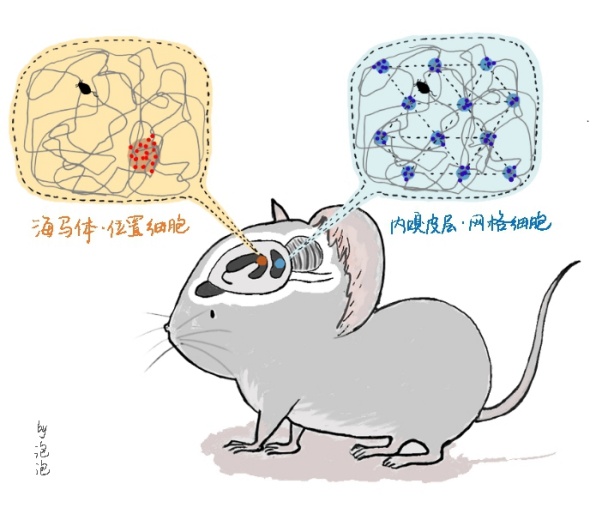
图4:海马区域的位置细胞和网格细胞负责大脑的导航与情景记忆
(图片来源:中国科学院脑智卓越中心官网)
那么,海马体是如何通过统一神经机制实现记忆形成与空间导航两大核心功能的呢?脑智卓越中心毛盾研究组在发表于Science Advances期刊的成果里给出了答案[3]。他们让猕猴先后完成记忆测试和自由导航任务,记录同一批神经元活动。发现了海马体里有专门管记忆和管导航的两类神经元,其中海马前端偏重于编码事物记忆,后端侧重于空间编码,分工明确。这一发现揭开了海马体双重功能的神秘面纱,也为理解灵长类脑功能提供了新视角。
调控情绪的关键,也最容易受疾病攻击
海马体在情绪调控中,扮演着一个关键而优雅的“接线员”角色。它并不直接产生强烈的恐惧或快乐,而是为你所经历的一切情绪事件赋予精确的时空背景和意义。当某件事引发强烈情绪时,情绪中枢杏仁核会迅速拉响警报,让你心跳加速,而就在此刻,海马体会记录下周围的情景,并将这些具体情境与当时的紧张感精密地捆绑在一起,形成一个完整的情景记忆。让你在未来面对类似情境时,能基于过去的完整记忆做出更恰当的反应。
正是海马体精准巧妙的情境绑定,将你掠过的情绪编织成了可追溯回味的人生印记。
在压力之下,身体会释放大量皮质醇等压力激素。短期应激时,这些激素能让海马体优先处理危机信息,然而一旦压力持续不断,过量的压力激素便会从“应急信使”转变为“神经毒素”,会逐渐干扰海马体神经元的能量代谢,甚至损害神经元之间那些重要的连接分支。久而久之,海马体编织记忆、整合情绪、绘制认知地图的核心功能会变得迟钝和混乱。所以,长期处于巨大压力下的人常常会感到记忆力下降、学习新事物困难,并且更容易陷入焦虑或无助的情绪中。
值得庆幸的是,海马体是大脑中少数具有显著可塑性的区域之一,当慢性压力解除,它的结构和功能往往能得到相当程度的恢复。因此,海马体实际上处于记忆与情绪的交汇点,它既被情绪所塑造,也深刻地影响着我们的情感世界。
海马体的这些功能并非一成不变,而是受到年龄、压力、疾病等多种因素的影响。海马体对缺血缺氧状态特别敏感,这使得海马体格外容易在多种脑部疾病中受损。
在阿尔茨海默病中,海马体是最先受到影响的大脑区域之一(图5)。患者表现为海马组织萎缩,记忆存储能力下降,核心症状是认知功能减退,并可能出现性格改变。长期高血压、动脉硬化等可能影响大脑供血,导致海马体因缺血而受损萎缩。脑部创伤也可能直接损害海马体结构,引发萎缩现象。病毒性脑炎常发生在海马部位,自身免疫性脑炎也会累及海马、边缘叶等区域,这些炎症疾病会对海马体造成损害,进而导致萎缩。此外,海马体还是癫痫发作的常见起源点。各种原因导致的海马硬化,都可能引起颞叶癫痫。
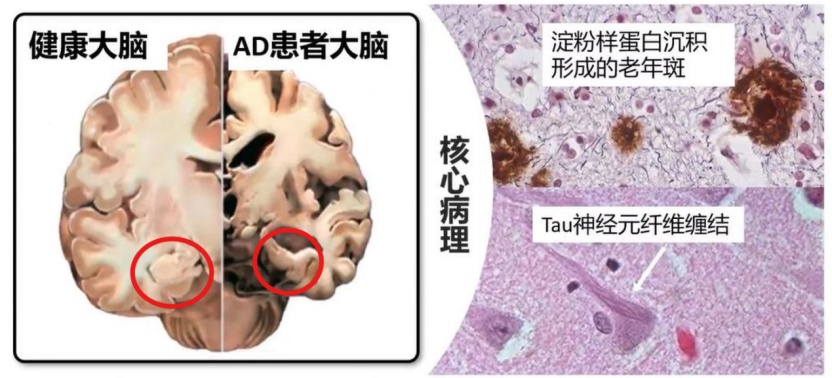
图5:受阿尔茨海默症影响的大脑(红圈内为海马体)
(图片来源:澎湃新闻)
脑智卓越中心徐春研究组通过稀疏标记结合荧光显微光学切片断层扫描技术,三维重构了上万个小鼠海马单神经元的全脑投射形态,建立了目前世界最大的海马单神经元全脑投射图谱数据集[4]。团队还通过机器识别算法分析,归纳出43种全脑投射细胞类型,揭示了海马神经元的空间联接规律及双侧大脑投射新机制。这些发现不仅为理解海马参与记忆、空间认知的神经环路基础提供了关键参考,也为阿尔茨海默病等记忆障碍疾病的机制研究提供了重要靶点。相关成果已发表在学术期刊Science上。
成年后,这里仍在产生新的神经元
传统观点认为,人类成年后大脑不会产生新的神经元。但近年研究发现,海马体是少数在成年后仍能产生新神经元的脑区之一(图6),这一过程称为成体神经发生[5,6]。当我们学习新知识、进行体育锻炼或者拥有丰富的环境体验时,能够激活位于海马体齿状回的神经祖细胞,促使它们分裂并逐渐发育成成熟的、能够传递信息的神经元,从而不断为大脑的神经网络增添新的活力[7,8]。
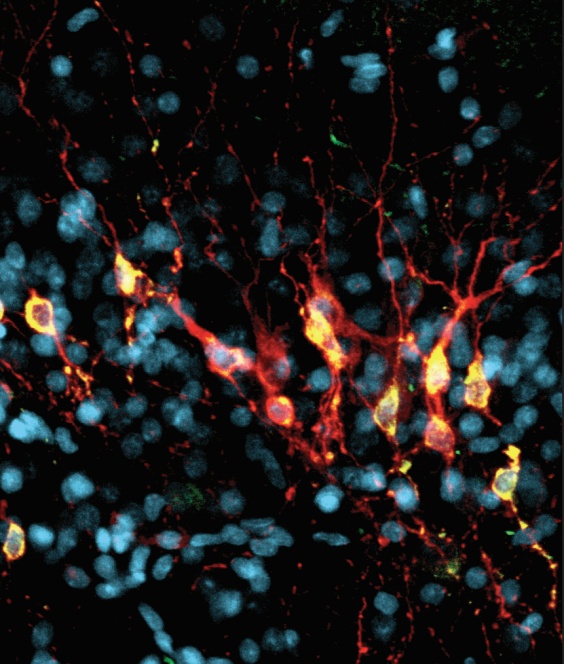
图6:人类海马体的新生神经元能够在成年时期调控学习记忆、认知、情绪等脑功能
(图片来源:脑智卓越中心周毅研究组)
脑智卓越中心周毅研究组在海马神经发生及脑发育领域取得了一系列的创新成果[9]。他们首次在成年人脑的单细胞测序数据中,直接识别出了这些成年才新产生的神经元,并绘制了从胚胎到老年,以及在阿尔茨海默病中,这些新生脑细胞的精细“分子地图”[7,10,11](图7)。他们进一步通过比较不同动物,他们发现了人类新生神经元独有的“配方”和演化秘密,这可能是我们大脑拥有独特能力的线索之一[12,13]。此外,他们还揭示了海马的成年神经干细胞如何被精准控制,从而增殖、分化成为神经元并迁移到正确位置的分子机制[14-16]。
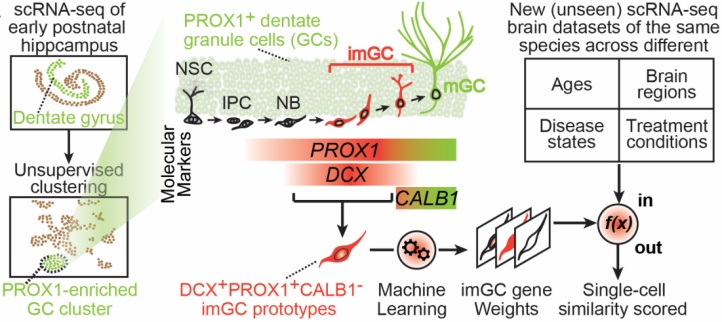
图7:通过单细胞组学测序并建立机器学习模型进行深度数据挖掘,首次绘制了人类海马体成体新生神经元的分子图谱
(图片来源:周毅研究组)
这些原创工作,为研究成年大脑如何“生长”打开了新窗口,也为全球科学家理解大脑发育、演化及相关疾病提供了宝贵的数据库和新分析方法。相关成果已发表在Nature、Nature Neuroscience、Cell Stem Cell(2篇)、Nature Reviews Genetics、PNAS等学术期刊。(PS:研究组诚挚邀请优秀的硕博研究生、博士后和本科生加盟团队。有兴趣者可点击文末“阅读原文”进一步了解。)
结语
海马体虽小,却是大脑中不可或缺的多面手。它是图书馆管理员,精心整理和保存记忆;又是导航员,帮助人们在空间中定向;是情绪调节师,维护心理健康;也是孜孜不倦的筑巢者,在成年阶段仍持续产生新生神经元,为大脑的可塑性与学习记忆能力不断注入新鲜活力。海马体以其独特的形态、持续的神经发生和关键的功能,成为大脑中最骏逸非凡的存在。
值此马年新春,祝愿所有科研工作者如海马体般深耕细作,在科研领域不断探索未知;祝愿每一位追梦人如新生神经元般蓬勃生长,在人生道路上收获满满记忆与成长。
作者简介
马卓然、周毅,中国科学院脑科学与智能技术卓越创新中心。
本文出品自“科学大院”公众号(kexuedayuan)。

科学大院是中国科学院官方科普微平台,致力于最新科研成果的深度解读、社会热点事件的科学发声
主办机构:中国科学院学部工作局
运行机构:中国科学院计算机网络信息中心
技术支持:中国科普博览
编辑:公子欣